Bu yazımızda toz şekerin özkütlesini (yoğunluğunu) bir deney yaparak bulacağız. Deneyi evde yapabiliriz. İhtiyacımız olan malzemeler toz şeker, 1 gram hassaslığında bir elektronik tartı ve sıvı hacmi ölçen dereceli bir kap ya da bardak. Özkütlenin ne olduğunu hatırlayalım, bir saf maddenin kütlesinin hacmine oranıydı. Şimdi bunu bir araştırma sorusu haline getirelim.
Araştırma sorusu ve hipotez
Şu iki sorudan birinin cevabını merak ediyoruz.
- Toz şekerin kütlesi hacmine göre nasıl değişir?
- Toz şekerin kütlesi ile hacmi arasındaki ilişki nasıldır?
Hipotezimiz de:
- Toz şekerin kütlesi hacmiyle doğru orantılıdır. Hacim arttıkça kütle de doğrusal olarak artar.
Deneyin tasarımı
Toz şekerin hacmini sıvıların hacmini ölçmekte kullanılan bir dereceli bardakla ölçebiliriz. Kütlesini de mutfak terazisi ile ölçebiliriz. Öyleyse bu deneyi yapmak oldukça kolay olacak. Aşağıda 50 mL için aldığımız ölçümün fotoğrafı gösteriliyor.

Değişkenler
Bağımsız değişken: Hacim. Çünkü toz şekerin hacmini biz değiştiriyoruz.
Bağımlı değişken: Kütle. Çünkü hacim değiştikçe ona bağlı olarak kütle değişiyor ve biz bu ilişkiyi merak ediyoruz.
Kontrol değişkenleri: Aynı bardağı kullanıyoruz ki kütleyi yanlış ölçmeyelim. Deneyi aynı ortamda yapıyoruz ki sıcaklık ya da basınç ölçümlerimizi etkilemesin.
Deneyin işlem basamakları
- Terazinin üstüne boş bardağı yerleştirip darasını alıyoruz, yani bardağın kütlesini ölçüm sonuçlarına katmasın istiyoruz.
- Bardağın içine bir kaşıkla 50 mL toz şeker dolduruyoruz.
- Terazinin gösterdiği değeri okuyup kaydediyoruz.
- İkinci ve üçüncü basamakları 100, 150, 200, 250, 300, 350 ve 400 mL toz şeker için tekrar ediyoruz.
Veri toplama
Aşağıdaki tablo bizim topladığımız veriyi gösteriyor.
| Kütle (g) | |
|---|---|
| 50 | 45 |
| 100 | 93 |
| 150 | 137 |
| 200 | 191 |
| 250 | 236 |
| 300 | 289 |
| 350 | 340 |
| 400 |
Veri analizi
Toz şekerin özkütlesini bulmak için tek bir ölçümün yeterli olduğunu düşünüyor olabilirsiniz. Ama farklı değerler için özkütleyi hesaplarsanız aynı çıkmadığını göreceksiniz. Örneğin V = 50 mL ve m = 45 g için d = 0,95 g/mL olurken V = 400 mL ve m = 379 g için d = 0,9 oluyor. Daha güvenilir bir değer bulmak için grafik çizmeliyiz. Özkütlenin tanımından bu grafiğe bir doğru oturtabileceğimizi ve doğrunun eğiminin özkütleyi vereceğini bekliyoruz. Ayrıca doğrunun ekseni 0,0 noktasında kesmesi gerektiğini de bekliyoruz (Peki neden? Cevaplarınızı yorumlarda bekliyorum.) Aşağıda toz şeker için kütle – hacim grafiği görülüyor. Noktalar bizim yaptığımız ölçümleri siyah doğru ise matematiksel modeli gösteriyor.
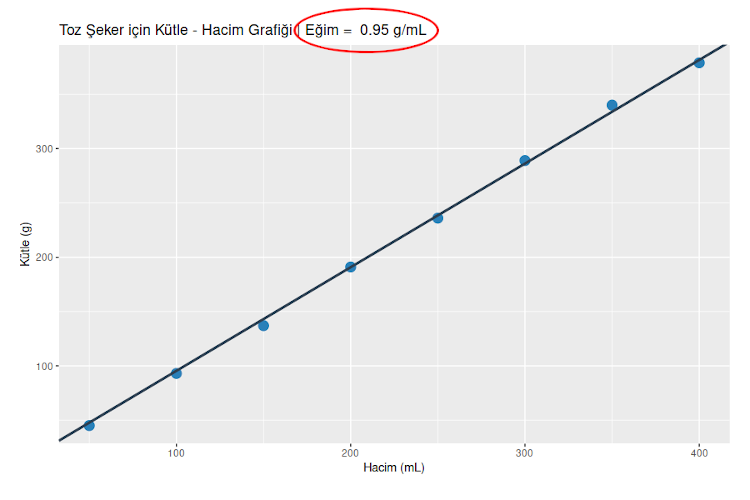
Toz şekerin özkütlesinin 0,95 g/mL olduğunu bulmuş olduk.
Sonuç ve değerlendirme
Araştırma sorumuza cevap bulabildik mi? Evet. Kütle ile hacim arasında doğru orantılı bir ilişki vardır. Hipotezimiz de tuttu. Hacim arttıkça kütle de doğru orantılı olarak arttı. Peki gerçekçi mi bulduğumuz değer? Dikkat edin bu suyun özkütlesinden küçük. Aslında toz şekerin özkütlesi 1,59 g/cm3. Bizim bulduğumuz değerin yaklaşık 1,7 katı. Neden böyle çıktı bizim değerimiz? Deneyde bir hata mı yaptık? Deneyi nasıl yaparsak referans değerine daha yakın bir değer elde edebiliriz? Bu sorular önemli, cevaplarınızı yorumlarda bekliyorum.
Deneyin videosu
Özkütle ile ilgili kazanımlar
9.2.1.1. Özkütleyi, kütle ve hacimle ilişkilendirerek açıklar.
- Sabit sıcaklık ve basınçta ölçüm yapılarak kütle-hacim grafiğinin çizilmesi; kütle, hacim ve özkütle kavramları arasındaki matematiksel modelin çıkarılması sağlanır. Matematiksel hesaplamalar yapılır.
- Kütle-özkütle, hacim-özkütle grafiklerinin çizilmesi ve yorumlanması sağlanır.
hocam (0,0) noktasından kesen bir doğru çizmemizin sebebi kütle ve hacim büyüklüklerinin skaler birer büyüklük olduğundan mutlak sıfır değerleri olması yani eksi bir değer alamadığından mı, bir de 0 ile 1 arasında da değerler olduğundan mı daha büyük bir noktadan çizmiyoruz?
diğer sorunun yanıtı da referans noktası belirli bir sıcaklık ve basınç altında belirlendiğinden bizim sıcaklık ve basınç değerlerimiz bunlardan farklı olduğu için midir? yazı için teşekkürler.
markadan markaya değişiyor. şeker kamışı ile şeker pancarından da farklı yoğunlukta toz şeker üretiliyor. sizinkinin marka ne? ve şeker pancarı mı?