Öz ısı (özgül ısı da denir) ve ısı sığası (ısı kapasitesi de denir) nedir sorusunu yanıtlamak için önce ısıyla sıcaklık arasındaki ilişkiyi anlamak gerekir. Bir sisteme ısı verildiğinde sistemin ya sıcaklığı artar ya da sistem hal değiştirir. Örneğin, kaynama noktasına ulaşmamış sıvı haldeki bir maddeye ısı verildiğinde sıcaklığı artar. Isı ve sıcaklık arasındaki ilişkinin matematiksel modeli şöyledir:
Q = mcΔT
Q verilen ısıyı, m maddenin kütlesini, c maddenin öz ısısını, ΔT sıcaklık değişimini gösterir.
ΔT = Tson – Tilk
şeklinde hesaplanır.
Öz ısı nedir?
Kütleleri eşit olan iki farklı madde aynı miktarda enerji aldığında ya da verdiğinde, bu maddelerin sıcaklıklarındaki değişim miktarları farklı olur. Isı ve sıcaklıkla ilişkili maddeler arasındaki bu farkı, öz ısı kavramı açıklar.
Öz ısı bir saf maddenin birim kütlesinin (1 kg ya da 1 g) sıcaklığını 1 °C (ya da 1 K) artırmak için verilmesi gereken ısı miktarıdır. Birimi J/kg°C ya da J/kgK olarak verilir ama cal/g°C da kullanılabilir. c (küçük harf c) simgesiyle gösterilir. Türetilmiş ve skaler bir büyüklüktür. Öz ısı maddenin ayırt edici bir özelliğidir.
Her maddenin öz ısısı farklıdır. Örneğin, 1 kg zeytin yağının sıcaklığını 1 °C artırmak için 1968 J ısı gerekirken, 1 kg suyun sıcaklığını 1 °C artırmak için 4186 J ısı vermek gerekir.
Ayrıca aynı maddenin farklı hallerinde öz ısı değişir. Örneğin, buzun (katı) öz ısısı 2100 J/kg°C, suyun (sıvı) 4186 J/kg°C, su buharının (gaz) öz ısısı 2010 J/kg°C’dir.
Aşağıdaki tabloda farklı maddelerin öz ısıları hem cal/g°C hem de J/kg°C cinsinden gösteriliyor.
| Madde türü | Öz ısı (cal / g°C) | Öz ısı (J / kg°C) |
|---|---|---|
| Su | 1 | 4186 |
| Buz | 0,5 | 2100 |
| Su buharı | 0,48 | 2010 |
| Zeytin yağı | 0,47 | 1968 |
| Etil alkol (0 °C de) | 0,55 | 2300 |
| Alüminyum (katı) | 0,21 | 880 |
| Demir (katı) | 0,11 | 448 |
| Bakır (katı) | 0,09 | 387 |
| Kurşun (katı) | 0,03 | 128 |
| Gümüş (katı) | 0,06 | 234 |
| Cıva (sıvı) | 0,033 | 140 |
| Cam | 0,2 | 840 |
Isı sığası nedir?
Isı sığası bir maddeye aktarılan ısının sıcaklık değişimine oranıdır. Herhangi miktarda bir maddenin sıcaklığını 1 °C (ya da 1 K) artırmak için verilmesi gerekli olan enerji miktarına ısı sığası denir. Isı sığasının tanımında, öz ısının aksine, kütle miktarına oran yoktur. Bu nedenle maddenin ayırt edici bir özelliği de değildir, kütle arttıkça ısı sığası artar. Isı sığası C (büyük harf C) ile gösterilir.
Q = mcΔT formülünü
mc = \frac{Q}{\Delta T}şeklinde yazarsak,
C = mc olarak tanımlarsak,
C ısı sığası anlamına gelir. Yani ısı sığası bir maddenin kütlesiyle öz ısısının çarpımına eşittir. Skaler ve türetilmiş bir büyüklüktür. Birimi J/°C veya J/K olarak verilir ama cal/°C olarak da kullanıldığı olur.
Bu durumda ısı sıcaklık ilişkisi formülü
Q =CΔT
şeklinde de yazılabilir.
Isı sıcaklık grafikleri
Öz ısı ve ısı sığası kavramlarını bir de grafik üzerinde görelim. Bunun için farazi bir deney verisi üzerinde çalışacağız. Su, zeytin yağı ve etil alkol kullanalım; her birinin kütlesi 2 kg olsun. Aşağıdaki tablolar her sıvı için verilen ısı miktarını ve sıvının sıcaklığını gösteriyor.
| Isı Q (kJ) | Su Sıcaklık T (°C) | Zeytin yağı T (°C) | Etil alkol T (°C) |
|---|---|---|---|
| 0 | 20 | 20 | 20 |
| 10 | 21,2 | 22,5 | 22,2 |
| 20 | 22,4 | 24,9 | 24,4 |
| 30 | 23,6 | 27,6 | 26,6 |
| 40 | 24,8 | 30,1 | 28,8 |
| 50 | 26 | 32,6 | 30,9 |
Şimdi bu tablodaki veriyi grafikte görelim:
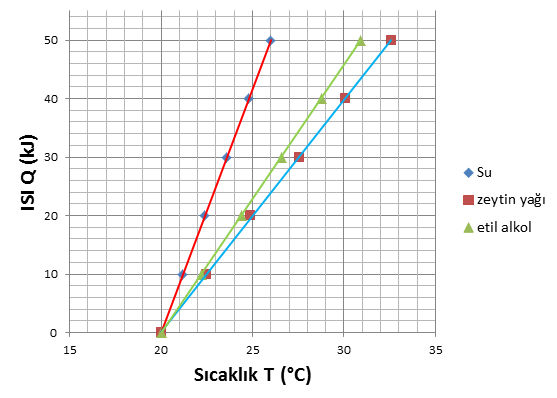
Sırayla bu üç sıvının grafiğini inceleyelim. Grafiğin eğimi bize ısı sığasını (C),
C=\frac{Q}{\Delta T}ısı sığasının kütleye oranı öz ısıyı (c) verir.
c = \frac{C}{m}Isının biriminin kJ (kilojoule) olarak verildiğine yani hesaplarda 1000 ile çarpmamız gerektiğine dikkat edin.
Su için öz ısı ve ısı sığası
Su için tablonun son ve ilk satırları arasındaki farkı alalım ve ısı sığasını hesaplayalım:
C_{su} = \frac{50 \space kJ}{26 ^\circ C-20 ^\circ C} C_{su} = \frac{50000 \space J}{6 ^\circ C}Csu = 8333 J/°C
Şimdi öz ısıyı hesaplayalım:
c_{su} = \frac{C_{su}}{m} c_{su} = \frac{8333 \space J/^\circ C}{2 \space kg}csu = 4167 J/kg°C
bulduk. Bu standart değer olan 4186 J/kg°C değerine oldukça yakın, deney hatalarından dolayı tam sonucu bulamamamız normal.
Zeytin yağı için öz ısı ve ısı sığası
Zeytin yağı için tablonun son ve ilk satırları arasındaki farkı alalım ve ısı sığasını hesaplayalım:
C_{zeytin \space yagi} = \frac{50 \space kJ}{32,6 ^\circ C-20 ^\circ C} C_{zeytin \space yagi} = \frac{50000 \space J}{12,6 ^\circ C}Czeytin yağı = 3968 J/°C
Şimdi zeytin yağının öz ısısını hesaplayalım:
c_{zeytin \space yagi} = \frac{C_{zeytin \space yagi}}{m} c_{su} = \frac{3968 \space J/ ^\circ C}{2 \space kg}czeytin yağı = 1984 J/kg°C
bulduk. Bu standart değer olan 1968 J/kg°C değerine epey yakın.
Etil alkol için öz ısı ve ısı sığası
Etil alkol için tablonun son ve ilk satırları arasındaki farkı alalım ve ısı sığasını hesaplayalım:
C_{etil \space alkol} = \frac{50 \space kJ}{30,9 ^\circ C-20 ^\circ C} C_{etil \space alkol} = \frac{50000 \space J}{10,9 ^\circ C}Cetil alkol = 4587 J/°C
Şimdi etil alkolün öz ısısını hesaplayalım:
c_{etil \space alkol} = \frac{C_{etil \space alkol}}{m} c_{etil \space alkol} = \frac{4587\space J/ ^\circ C}{2 \space kg}cetil alkol = 2294 J/kg°C
bulduk. Bu standart değer olan 2300 J/kg°C değerine yakın.
Öz ısı ve ısı sığası örnek sorular ve çözümleri
Örnek Soru 1
Kütlesi 30 g olan bir gümüş külçenin sıcaklığını 15 °C’den 80 °C’ye çıkarmak için kaç J ısı gereklidir? (Gümüşün öz ısısı 234 J/kg°C ‘dir.)
Çözüm:
Isı, kütle, öz ısı ve sıcaklık arasındaki ilişkiyi gösteren formülü yazalım:
Q = mcΔT
Kütleyi kg’ye çevirelim.
m = 30 g = 0,03 kg
Sıcaklık farkını bulalım.
ΔT = Tson – Tilk
ΔT = 80 °C – 15 °C = 65 °C
Q=0,03 \space \cancel{kg} \times 234 \frac{J}{\cancel{kg} \cancel{ ^\circ C}} \times 65 \space \cancel{ ^\circ C}Birimlerin birbirini götürüp ısı birimi olarak J kaldığına dikkat edin.
Q = 456,3 J
Örnek Soru 2
Kütlesi 0,5 kg olan bir maddeye 17600 J ısı verildiğinde sıcaklığı 40 °C artıyor. Bu maddenin ısı sığasını ve öz ısısını hesaplayın.
Çözüm:
Önce öz ısıyı bulalım:
Q = mcΔT
m = 0,5 kg
ΔT = 40 °C
17600 J = 0,5 kg x c x 40 °C
17600 J = 20 kg°C x c
c = \frac{17600 \space J}{20 \space kg ^\circ C}c = 880 J/kg°C
Bu hangi madde olabilir? Nasıl bulabilirsiniz? Yorumlarda cevap verebilirsiniz.
Şimdi ısı sığasını bulalım:
C = mc
C = 0,5 kg x 880 J/kg°C
C = = 440 J/°C
Örnek Soru 3
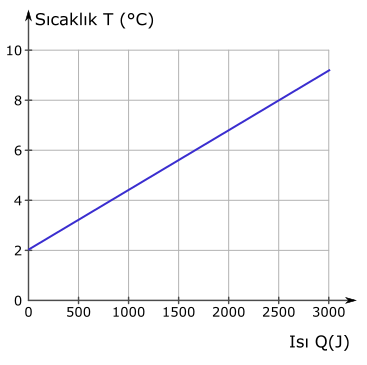
Yukarıdaki grafikte gösterilen maddenin ısı sığası kaç J/°C’dir? Bu maddenin kütlesi 2 kg ise öz ısısı ne kadardır?
Çözüm:
Isı sığası C = Q/ΔT olarak tanımlanıyordu.
Bu grafikteki mavi çizginin üstünde öyle bir nokta bulmalıyız ki sıcaklık değişimini de ısıyı da net bir şekilde okuyabilelim. Bu nokta mavi çizginin karelerin köşesiyle kesiştiği yerde olmalı. (2500 J, 8 °C) aradığımız nokta. Artık hesaplamayı yapabiliriz.
Q = 2500 J
ΔT = Tson – Tilk
Başlangıç sıcaklığının 2 °C olduğuna dikkat edin.
ΔT = 8 °C – 2 °C = 6 °C
C = 2500 J/ 6 °C
C = 416,7 J/°C
Şimdi de öz ısı ne kadarmış onu bulalım.
C = mc
c = C/m
m = 2 kg
c = \frac{416,7 \space J/ ^\circ C}{2 \space kg}c = 208,3 K/kg°C
Öz ısı ve ısı sığası ile ilgili Kazanımlar
9.5.1.4. Öz ısı ve ısı sığası kavramlarını birbiriyle ilişkilendirir.
- Günlük hayattan örnekler (denizlerin karalardan geç ısınıp geç soğuması gibi) verilir.
9.5.1.5. Isı alan veya ısı veren saf maddelerin sıcaklığında meydana gelen değişimin bağlı olduğu değişkenleri analiz eder.
- Deney veya simülasyonlardan yararlanılarak değişkenler arasındaki ilişkiyi belirlemeleri sağlanır. Matematiksel model verilir. Matematiksel hesaplamalara girilmez.
bu j/gr°c nıye değil
Kütlenin SI birimi kg olduğu için.
“Isı sığasının tanımında, öz ısının aksine, kütle miktarı yoktur.”
ifadesi yanlış yazılmış sanırım. Isı sığası C=mc olarak tanımlandıysa kütleye bağlıdır ve farklı maddelerin ısı sığası kütlelerin öz ısısıyla aynı k değerine sahip olacak şekilde belirlenebilir. Bu yüzden C ayırt edici özellik değildir.
Bu arada konu anlatımı çok iyi hocam, teşekkürler.
“Isı sığasının tanımında, öz ısının aksine, kütle miktarına oran yoktur.” şeklinde düzeltildi. Dikkatiniz harika teşekkürler.
3. soruda ısı sığasını bulalım diyorsunuz C=mc diyorsunuz 4 soruda öz ısısını bulalım diyorsunuz C=mc diyorsunuz öz ısıyla ısı sığası aynı şey mi
Öz ısı = Isı sığası / kütle, ilişkili şeyler ama aynı şey değiller.
Hocam bazı grafiklerde zaman ekseninin bulunduğu yere ısı ekseni de yazıyorlar bunun nedeni nedir açıklarsanız sevinirim 🙂
Genelde grafiklerde ısı-sıcaklık kullanılır. Ama bazen zaman-sıcaklık olarak verilebilir. Zaman, birim zamanda sabit miktarda ısı verildiği varsayımını gösterir. Yani büyük bir fark olmaz genelde.
hocam son örnek soruda Tson demişsiniz sonda 8 değilde grafikte 9 derece de durmuş ama siz Tson-Tilk yazdığınızdaa 8-2 yazmışsınız 9-2 olmayacak mı
Biz eğim arıyoruz. Mavi çizginin karelerin köşesiyle kesiştiği yerde bir nokta seçmeliyiz. (2500 J, 8 °C) aradığımız nokta.
Isı sığası ,ısı biriktirme kapasitesi midir
Bir anlamda öyle diyebiliriz.
Hocam peki öz ısının tanımında saf oluşu önemli midir başta ozisinin tanımında belirtmissiniz ama cam örneği kafa karıştırıyor.ozisi saf, isi sığası karışım icin geçerli diyebilirmiyiz kütlenin aksine.
Hayır. Burada hem özısı hem de ısı sığası için sadece saf maddelerden bahsediyoruz. Camı saf madde kabul ediyoruz.
200 gr suyun sıcaklğını 10 dereceden 20 dereceye çıkartmak için suya verilmesi gereken ısı miktarı kaç cal olur? ( suyun özısısı 1 cal/gr)
yardımcı olur musunuzzz???
İLK BAŞTAKİ AÇIKLAMANIZDA BİR SİSTEME ISI VERİLDİĞİNDE SİSTEMİN YA SICAKLIĞI ARTAR YA DA HAL DEĞİŞTİRİR DEMİŞSİNİZ ANCAK İKİSİNİN AYNI ANDA OLDUĞU ANLAR YOK MUDUR?